
7月31日,恒瑞医药宣布PD-1卡瑞利珠单抗联合甲磺酸阿帕替尼片(“双艾”组合)的BLA获FDA正式受理,拟用于不可切除或转移性肝细胞癌患者的一线治疗。
这算是恒瑞医药在美国市场正式的第一个生物制品上市申请,恒瑞作为国内医药行业的标杆企业,其全球化布局时刻牵动着众多医药行业投资者的神经。
那么,恒瑞医药的“双艾组合”,出海胜算如何?不妨理性分析。
01 美国的肝癌治疗标准
据世界卫生组织(WHO)2020年统计的数据显示,全球有90万人被诊断患有肝癌,83万人死于肝癌,不仅是全球第六大最常见癌症,亦是全球癌症死亡相关第三大原因。
以2020年为例,美国当年患肝癌的人数大约为3.3万,因肝癌死亡的人数为2.6万。
尽管美国拥有全球最好的肝癌治疗条件,但依旧缺乏能够显著延长晚期肝癌患者生存期的出色治疗手段。在美国,肝癌的一般5年生存率为20%;对于早期诊断为肝癌的43%的人来说,5年生存率为35%;若癌症已扩散到周围组织或器官,5年存活率为12%;若已扩散到身体的远处,5年存活率是3%。
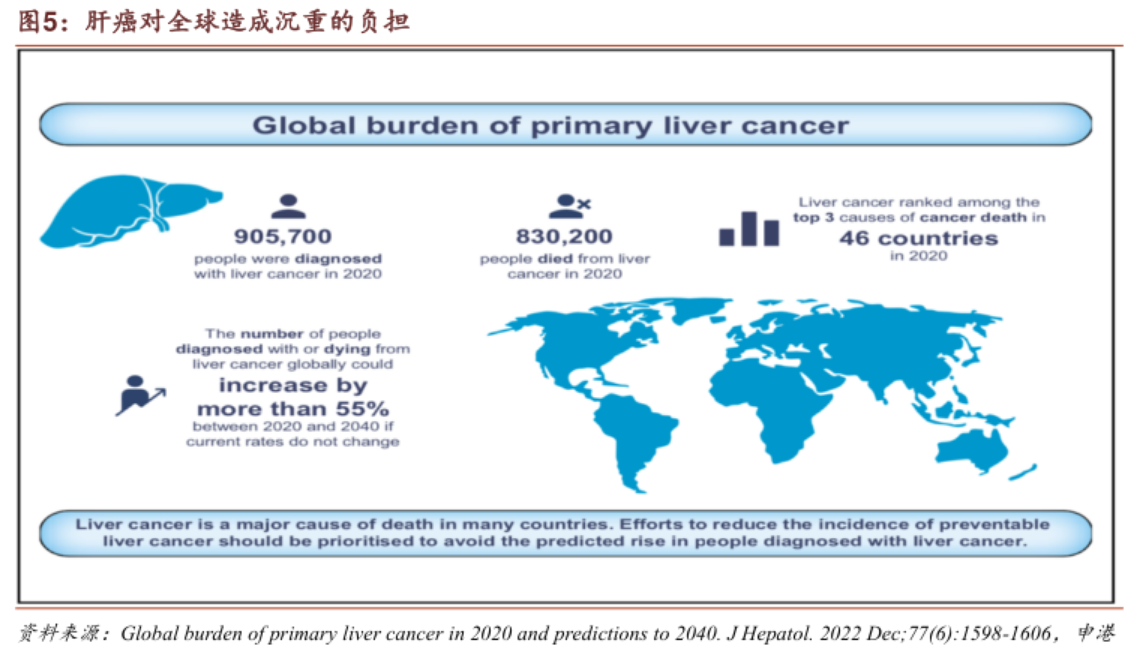
肝细胞癌治疗包括外科治疗、肝移植、局部消融、全身治疗等方式,其中手术切除适用于早期病人(占肝癌患者20-30%),且为肝癌唯一可能治愈的手段;不过,基于手术切除病人约70%五年内出现复发、80%肝癌患者一经发现便已是晚期的数据,针对晚期肝癌患者的全身治疗方式更受业内关注。
在最新版的美国NCCN晚期肝细胞癌治疗指南中,目前肝癌的一线全身治疗方案一共有6个,首选方案是阿替利珠单抗+贝伐珠单抗(T+A),在其他一线备选方案中,一线靶向单药治疗可使用索拉非尼或仑伐替尼,一线免疫单药治疗也增加了度伐利尤单抗和帕博利珠单抗。
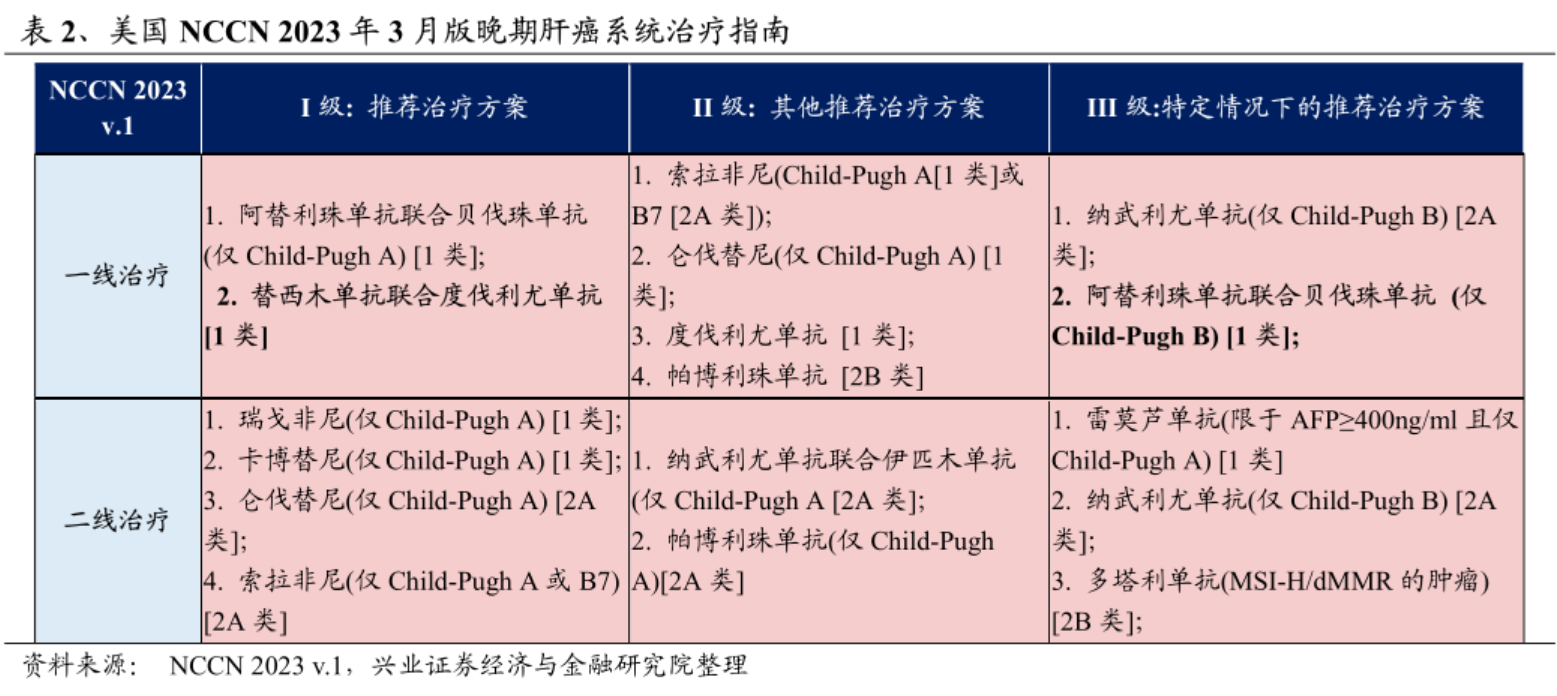
索拉非尼一度是美国一线晚期肝癌患者被首要推荐的标准疗法,其对于一线不可切除的晚期肝细胞癌患者疗效,患者中位无进展生存期大约在4-5个月,中位总生存期在13-15个月。
T+A已经在多个临床试验中证明其相比索拉非尼在一线晚期肝癌患者治疗中具备PFS、OS双优效,患者中位无进展生存期大约在5.5-7个月,中位总生存期在19-24个月。
02 双艾组合令人惊艳之处
恒瑞的“双艾组合”CARES-310研究于2018年12月获得CDE、FDA批准在全球开展临床试验,这项试验由全球13个国家和地区的95家中心共同参与,研究的主要终点是无进展生存期(PFS)和总生存期(OS)。
CARES-310研究结果显示:相比活性对照组,组合疗法显著改善了中位PFS(5.6个月 vs 3.7个月;HR:0.52;单侧p<0.0001);中位OS也获得显著延长(22.1个月 vs 15.2个月;HR:0.62;单侧p<0.0001)。
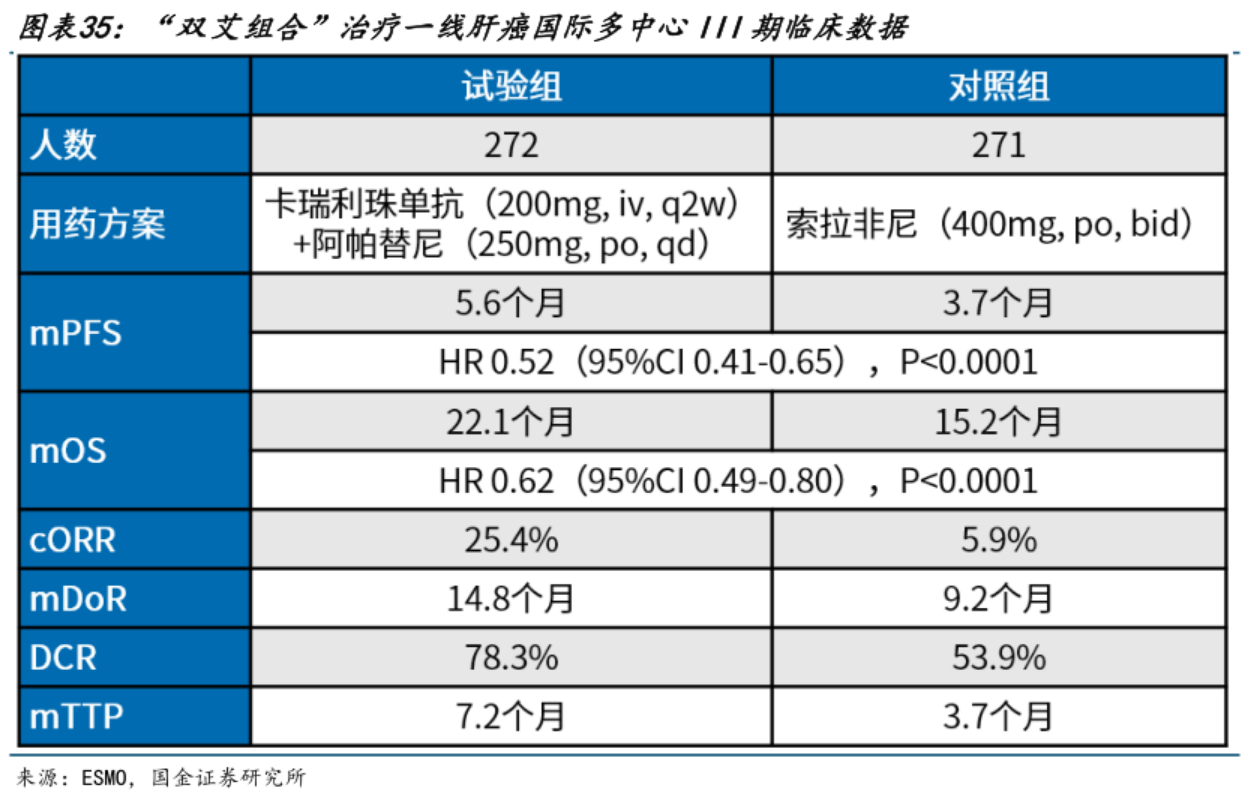
之所以能够取得如此强有力的临床数据,离不开“双艾组合”的治疗协同机制。
PD-1卡瑞利珠单抗,可以抑制PD-1与PD-L1的结合,恢复T细胞对肿瘤的杀伤能力,并增强机体免疫系统功能;阿帕替尼则是一种靶向药物抗血管生成抑制剂,可以抑制肿瘤血管再生及癌细胞生长。
两款药物的结合,目前已经证明了“1+1>2”的潜力。一方面,阿帕替尼能够阻断肿瘤细胞生成新的血管、限制肿瘤的氧气和营养物质供给,改善肿瘤微环境;另一方面,卡瑞利珠单抗重新激活受限的T细胞,使T细胞大量富集于肿瘤细胞周围,起到更好的杀伤作用。
双艾组合的作用机制提升临床获益,可能具备一定的广谱性。据最新研究显示:肺癌、肝癌、宫颈癌及消化道肿瘤患者经双艾组合的治疗,均能获得一定的生存期获益。如哈佛大学一项黑色素瘤研究结果显示:双艾组合治疗17%的完全缓解率高于卡瑞利珠单抗单药治疗的6%。
03 一些影响审批的不确定性
尽管FDA已经受理了双艾组合一线治疗不可切除或转移性肝细胞癌患者的上市申请(BLA),但距离获批仍存在不少的挑战,我们不妨理性分析。
首先,双艾组合强劲的疗效掩盖了安全性数据的一些瑕疵。
CARES-310研究结果显示,双艾组合的3级或4级治疗不良反应发生率为80.5%,最常见相关不良事件为高血压(组合疗法vs活性对照组:38% vs 15% ),双艾组合治疗组有1例患者发生治疗相关死亡(多器官综合症)。
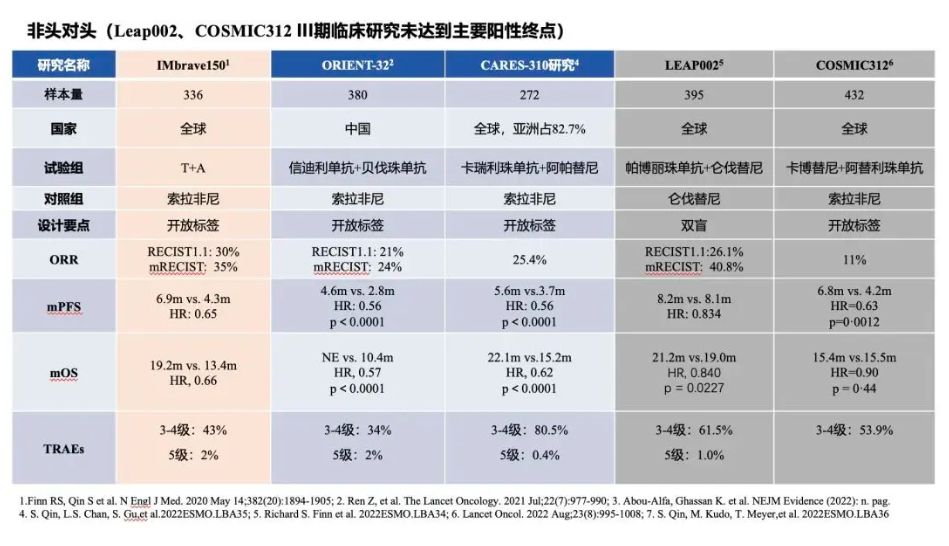
横向比较T+A组合、K药+仑伐替尼三期临床数据(选取了中位OS获益相近的试验),双艾组合的3-4级不良反应发生率数据最高。假如双艾组合真能顺利获批,也可能被赋予黑框警告。
其次,CARES-310研究的入组患者多样性市场也存在一定疑虑。
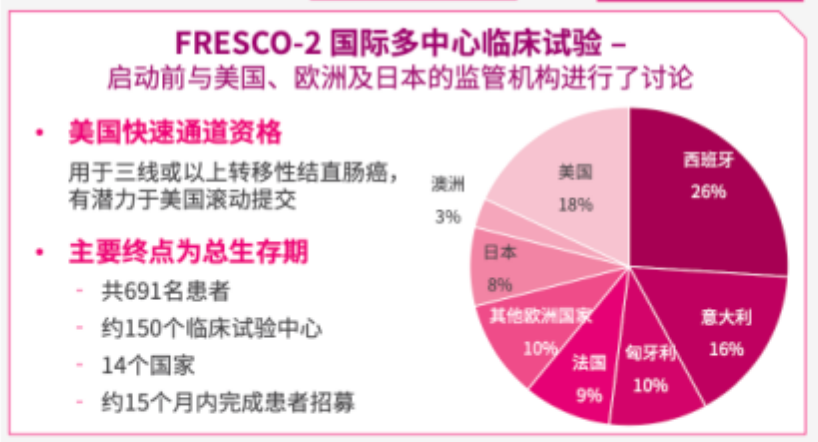
拒公开资料显示,CARES-310研究是以中国肝癌患者为基础的全球三期随机对照临床研究,亚洲患者占入组患者的82.7%,其中70%以上来自中国大陆,也就意味着欧美人群占入组患者不足20%。
通常FDA是不允许用单一国家,且是与美国的种族谱很不同的国家的临床试验数据来支持在美国上市申请的。某PD-1企业的业绩交流会曾经透露过:FDA要求PD-1至少30%入组患者来自于欧美国家。
以和黄医药的呋喹替尼为例,之所以获得武田的认可,除了药物卓越的疗效和安全性,其全球多中心入组人群的多样性也增加了该药获批的“赔率”。
但特殊情况下这条通例可以被打破,比如前沿性全新的药品、在欧美地区难以入组患者、临床大量未满足需求等,比如鼻咽癌、肝细胞癌、脑胶质瘤均属于罕见病。
最后,便是CARES-310研究对照组设计问题,要看FDA如何看待。
CARES-310研究的对照组药物是索拉非尼单药,尽管在PFS、OS做出了双优效,当时的晚期肝癌一线推荐治疗用药也的确是索拉非尼,但仍然存在隐忧。
2020年5月,发表在著名权威期刊《新英格兰医学杂志》上的报道显示,“T+A”联合用药方案和索拉非尼相比,显著改善了肝癌患者总生存率。2021年,美国2021版肝胆癌NCCN指南“T+A”组合替代索拉非尼成为指南推荐中唯一的一线治疗优选方案。
由于“T+A”组合治疗一线晚期肝癌患者获益相比索拉非尼十分显著,如果恒瑞医药的双艾组合对照的是“T+A”取得优效结果那自然没有这个问题,而双艾组合对照的是索拉非尼,这就要看FDA如何看待。
近日,CDE发布了三份药物临床试验相关的技术指导原则(以患者为中心的临床设计、临床实施技术、风险评估),强调未来创新药物临床设计,需要要结合未来一段时间的治疗方式变革,去动态的评估和选择最优对照组,这项政策的灵感不知道是否源于欧美。
双艾组合的出海,仍然悬而未决,市场充满了欢快的讨论气息。
结语:只局限于国内,恒瑞医药毕生只能成为中国的Big pharma,公司急需一个出海来打破公司的天花板。未来,是双艾,还是ADC呢?

 下载APP
下载APP










 下载APP
下载APP

